MIELOFIBROSIS [ICD-10: (M9961/1) D47.1] |
|
|
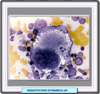
La mielofibrosis primaria es un trastorno crónico, generalmente idiopático, caracterizado por fibrosis de la médula ósea, esplenomegalia y anemia con glóbulos rojos inmaduros de en forma de lágrima (dacriocitos) (*). Suele estar acompañada por hematopoyesis extramedular (*) . Es una enfermedad poco común que afecta a 2 personas/millón. Se suele diagnosticar entre los 50 y 80 años, pero puede ocurrir a cualquier edad, y afecta tanto a hombres como a mujeres. Aunque en muchos casos se ignora la etiología de esta enfermedad, en un 50% de los casos está presente una mutación del gen JAK2 (*) y en un 10% una mutación del gen MLP. La enfermedad se presenta como mielofibrosis primaria o secundaria, en este caso como transformación de una policitemia vera o una trombocitemia esencial previas. Ambos tipos de mielofibrosis se incluyen en la llamada mielofibrosis con metaplasia mieloide. La mielofibrosis afecta la producción de glóbulos rojos, glóbulos blancos y plaquetas. Se elaboran muy pocos eritrocitos (muchos de ellos como dacriocitos) y, por lo general, demasiados leucocitos y plaquetas. Una característica constante importante de la mielofibrosis es la producción excesiva de megacariocitos, algunos de estos anormales. Puede ocurrir entonces que se produzca un exceso de plaquetas (trombocitemia) o, por el contrario un defecto de las mismas. En el primer caso, el exceso de plaquetas hace que se liberen citokinas, las cuales estimulan la producción de tejido fibroso en la médula. |
||
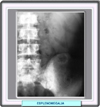
SINTOMAS La síntomatología de la mielofibrosis tiene tres componentes fundamentales: la anemia (con astenia y disnea de esfuerzo), la esplenomegalia (con molestias en el hipocondrio izquierdo) y el estado de hipermetabolismo secundario a la mieloproliferación (anorexia, pérdida de peso, sudación nocturna, crisis de gota, litiasis renal). Algunos pacientes presentan diátesis hemorrágica. Sin embargo, en un 25% de los casos no hay síntomas y el diagnóstico se efectúa de forma casual. El dato más frecuente de la exploración física es la esplenomegalia, que puede ser confirmada radiológicamente, o por ultrasonografía o tomografía. Cuando la hematopoyesis extramedular es exuberante pueden aparecer ascitis, hipertensión pulmonar, obstrucción intestinal o ureteral, hipertensión intracraneal, taponamiento cardíaco, compresión medular o nódulos cutáneos. En un 80% de los casos, también se observa hepatomegalia. Las adenopatías, raras al inicio de la enfermedad son algo más frecuentes en los casos de larga evolución en los que también se pueden observar nódulos cutáneos. En el frotis sanguíneo aparecen los rasgos característicos de la hematopoyesis extramedular: eritrocitos en forma de lágrima, eritrocitos nucleados, mielocitos y promielocitos; también puede haber mieloblastos pero no tienen significación pronóstica. En el aspirado de la médula ósea (cuando ello es posible) se descubre una hipercelularidad medular con hiperplasia de las tres líneas celulares y en particular megacariocitos aumentados, pero sin las típicas alteraciones morfológicas que distinguen a la mielofibrosis idiopática crónica de los otros procesos mieloproliferativos crónicos. La presencia de más de un 25% de blastos es consistente con el diagnóstico de mielofibrosis. Los análisis citogenéticos se utilizan para descartar otros desórdenes mieloproliferativos asociados a la fibrosis mieloide (p.e la ausencia de BCR-ABL1 permite descartar una leucemia mielocítica pH+, mientras que el JAK2V617F está presente en el 50% de los casos de mielofibrosis). En las biopsias medulares se observan cuatro lesiones fundamentales: hiperplasia hematopoyética, fibrosis reticulínica, fibrosis colágena y osteosclerosis. En el examen de la sangre periférica suele observarse anemia normocítica y normocrómica. Son frecuentes los dacriocitos, e igualmente es característico el síndrome leucoeritroblástico, caracterizado por la presencia de eritroblastos y células mieloides inmaduras (mielocitos, metamielocitos, y raras veces blastos y promielocitos). La cifra de leucocitos es muy variable y oscila entre la leucopenia y una leucocitosis intensa. Lo mismo ocurre con las plaquetas, ya que en un 20% de los casos se observa trombocitopenia y en el 25% de los casos trombocitosis Las alteraciones bioquimicas más comunes son aumentos de la LDH, ácido úrico y vitamina B12. Con cierta frecuencia se detectan anticuerpos antinucleares y se observa positividad en el test de Coombs. TRATAMIENTO Hasta hace muy poco tiempo, el único tratamiento de la mielofibrosis era el paliativo, en particular el relativo a la esplenomegalia y la anemia. Cuando es progresiva, la esplenomegalia debe ser tratada para evitar el desarrollo de una hiperplasia intratable. Se han utilizado fármacos citotóxicos como el busulfan, melfalan, clorambucilo, 6-tioguanina e hidroxiurea, está ultima siendo el más utilizado por ser el mejor tolerado. Sin embargo, sólo se consigue un 40% de respuestas clínicas y estas duran tan solo 4.5 meses. También se ha utilizado el interferon b, pero este suele ser mal tolerado. Se ha utilizado también la irradiación del bazo con fracciones de 0.5 a 1 Gy administradas diariamente o de forma intermitente. Igual que en el caso anterior, la respuesta es pasajera (3.5 meses de duración) y la toxicidad hematopoyética es a menudo importante. Muchos pacientes con mielofibrosis muestran una deficiencia en vitamina D, mejorando su sintomatología cuando se administra esta vitamina. La esplenectomía puede estar indicada en pacientes con esplenomegalia dolorosa, infartos esplénicos recurrentes, anemia dependiente de transfusiones o trombocitopenia. Aunque ocasionalmente se observa mejoría de la anemia, este procedimiento está asociado a una morbilidad del 15 al 30% y a un índice de mortalidad del 10% debido sobre todo a infecciones, hemorragias y trombosis. Además, en un 20% de los pacientes se desarrolla hepatomegalia y trombocitosis después de la esplenectomía.
|
|||
|
|
|||
La anemia responde favorablemente en un 40% de los casos a un tratamiento con esteroides anabólicos como el danazol. De igual manera, la eritropoyetina produce respuestas aceptables en un 16-64% de los pacientes. Sin embargo, ambos fármacos podrían ser inductores de una transformación leucémica de la mielofibrosis
|
|||
El trasplante alogénico de células madre de médula osea es, por el momento, el único tratamiento curativo de la mielofibrosis con metaplasia mieloide. Varios estudios retrospectivos sobre los resultados del trasplante de médula han puesto de manifiesto que, hasta 1996, la mortalidad asociada al procedimiento era del 30% y el riesgo de rechazo del 10%, por lo que existe una cierta prevención para llevar a cabo este procedimiento. Además, algunos autores estiman que la médula ósea fibrosa es un mal receptor del trasplante. A partir de 1996, se ha conseguido una reducción de la mortalidad asociada al trasplante alogénico gracias a la posibilidad de una mejor elección del donante, el estudio del quimerismo linfohematopoyético, y la disponibilidad de una quimioterapia más efectiva antes y después del trasplante.
|
|||
La lenalidomida es un derivado de la talidomida, que inhibe varias de las citokinas que intervienen en los procesos inflamatorios, entre ellas el factor de necrosis tumoral. Administrada en dosis de 10 mg/día durante 3 o 4 meses a pacientes con mielofibrosis con metaplasia mieloide, mejora la anemia en el 22% de los casos, la esplenomegalia en el 33% y la trombocitopenia en el 50%. Además, en algunos pacientes se observó la remisión de la leucoeritroblastosis, una reducción de la fibrosis y angiogenesis óseas y ocasionalmente una remisión citogenética con una reducción en la carga de la mutacion JAK2V617F En combinación con prednisona, la lenalidomida en dosis de 10 mg/dia durante ciclos de 21/28 días ha ocasionado una reducción de la anemia y de la esplenomegalia en un número significativo de pacientes. Lo más interesante de este reciente estudio es la regresión de la fibrosis ósea de grado 4 a grado 2 y el hecho de que en todos los pacientes con mutación JAK2(V617F) la carga de la proteína mutada se redujo en más del 50%
|
|||
|
En los últimos años se ha prestado un especial interés al desarrollo de inhibidores de la proteina kinasa Jak2. Varios fármacos se encuentran en fase de desarrollo, entre ellos el lesaurtinib. Este fármaco ha sido ya estudiado en pacientes con mielofibrosis, la mayoría de ellos con esplenomegalia, siendo el 36% de los mismos dependientes de transfusiones periódicas. En este estudio, se ha obtenido una respuesta positiva en el 27% de los pacientes a los 3 meses de tratamiento, aunque no hubo cambios en la fibrosis medular ni en la citogenética. Actualmente (2010) se están estudiando dosis mayores de este fármaco. El INCB018424 es un potente y selectivo inhibidor de la Jak1 y Jak2, no afectando a la mayoría de las otras kinasas estudiadas. En los estudios preclínicos, este fármaco inhibió el crecimiento de células BaF/3 con la mutación JAK2 y células CD+34 de pacientes con policitemia vera, sin afectar a otras líneas celulares. En los modelos animales portadores de la mutación JAK2V617F, el tratamiento con el INCB018424 ocasionó una reducción significativa del tamaño del bazo y una caída espectacular de las citokinas circulantes IL-6 y TNF-a, ambas implicadas en la patogenesis de las enfermedades mieloproliferativas. En los varios estudios clínicos de fase I y II realizados con el INCB018424, con dosis iniciales de 25 mg dos veces al día escalando la dosis hasta 400 mg/dia se ha comprobado una reducción sin precedentes del tamaño del bazo y una mejoría importante de los síntomas constitucionales de la mielofibrosis. El desarrollo de trombocitopenia ha sido el factor limitante en el escalado de las dosis. Hasta el momento (enero 2010) los investigadores han observado en 150 pacientes importantes beneficios clínicos que se han mantenido durante más de un año.
|
||
| Este fármaco, denominado ruxolitinib ha sido aprobado en 2011 sobre la base de los estudios COMFORT I y COMFORT II. | |||
REFERENCIAS
|
|||
|
|||
| Monografía revisada el 8 de Junio de 2013. Equipo de Redacción de IQB | |||

|
|||
|
|
|||