|
AEROSOLES ANTICOLINÉRGICOS |
 |
|
Se definen como anticolinérgicos una serie de sustancias, naturales o de síntesis que inhiben los efectos de la acetilcolina sobre el sistema nervioso central y periférico. Son inhibidores reversibles de los dos tipos de receptores colinérgicos: los muscarínicos y los nicotínicos, siendo la mayor parte de los anticolinérgicos que actúan sobre las vías respiratorias antagonistas del receptor muscarínico.
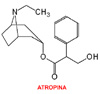
Los fármacos anticolinérgicos cuyo exponente conocido desde más antiguo es la atropina (*) eran conocidos ya en la antiguedad. La atropina se encuentra presente en la Atropa belladona L (*) una planta solanácea ya conocida en la epoca de los romanos - se dice que Claudio fue envenenado con tintura de belladona añadida a un plato de setas, su plato favorito -- y de los celtas que la utilizaron para envenenar cerveza que ofrecieron a sus invasores daneses. En la época romana, las damas se aplicaban sobre la cara preparados de belladona para aumentar el tamaño de sus pupilas, siendo debido el nombre de Atropa belladona otorgado por Lineo, a sus propiedades como veneno - Atropos es la mas vieja de las tres Parcas, que corta el hilo de la vida - y como embellecedor de las mujeres "belladona". Otras muchas plantas y setas venenosas contienen alcaloides con propiedades anticolinérgicas como la Datura stramonium (*) , conocida hace ya más de 4000 años por los indios americanos del Sur de Tejas y descrita como planta alucinógena en el hinduismo ayurvédico. La datura contiene, además de atropina, hioscina y escopolamina. Finalmente, el beleño negro (*) (Hyosciamus niger), cuya tintura fué utilizada por Shakespeare para matar a Hamlet, contiene sobre todo hiosciamina y escopolamina.
Los indios aspiraban el humo de la belladona como tratamiento de afecciones respiratorias y la observación de esta práctica por los ingleses condujo en el siglo XIX a la introducción de esta planta para el tratamiento del asma. Así, el Codex fr. de 1904 describe "el cartón antiasmático" a base de belladona y estramonio en polvo que se quemaba durante los accesos de asma. En 1833, el químico alemán identificó en los extractos de belladona el principio activo que producía los efectos midriáticos. Los efectos farmacológicos de la atropina fueron estudiados en la segunda mitad del siglo XIX, pero no fué hasta la década de los 30 del siglo pasado cuando se demostró que la actividad parasimpaticolítica de la atropina y de los otros alcaloides naturales se debían a sus efectos sobre los receptores colinérgicos.
Receptores colinérgicos
La acetilcolina, estudiada desde comienzos del siglo XX, es el neurotransmisor mejor conocido. Es una molécula pequeña presente en casi todos los tejidos, que se sintetiza a partir de la serina sobre todo en las terminaciones presinápticas ganglionares y en los terminales postgangliónicos del parasimpático. La acetilcolina se almacena en unas vésiculas sinápticas, pequeños orgánulos de unos 40 nm de diámetro que se acumulan en la región presináptica de la terminal del axón. Cuando llega un estímulo nervioso, la acetilcolina es liberada de estas vesículas, cruzando la hendidura sináptica y fijandose en los receptores colinérgicos de la célula adyacente.
Se conocen
dos tipos de receptores colinérgicos: los nicotínicos
(llamados así porque muestran alta afinidad hacia la nicotina,
un alcaloide del tabaco) y los muscarínicos (que fijan la muscarina,
un alcaloide presente en el hongo tóxico, la Amanita phalloides).
Estos receptores modulan un gran número de procesos del sistema
nervioso central y periférico y su inhibición o estimulación
regulan la actividad simpaticomimética o simpaticolítica.
Prácticamente, son los únicos receptores colinérgicos
que se encuentran presentes en los pulmones y las vías aéreas. |
|
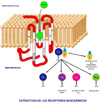 |
Los receptores muscarínicos son receptores metabotrópicos de membrana acoplados a proteínas G pertenecientes a la superfamilia de receptores que poseen 7 regiones transmembrana y que son ligandos para un gran número de neurotransmisores y hormonas que se fijan a las regiones transmembrana externas a la célula (*). Esta unión ocasiona una serie de modificaciones conformacionales del receptor, modificaciones que constituyen la señal que transmite a las proteínas G unidas al receptor. A su vez, estas proteínas G desencadenan una cascada de eventos que finalizan en una estimulación de la función de las células diana. Por ejemplo, la llegada de un agonista como la acetilcolina a un receptor muscarínico situado en una célula muscular lisa, por ejemplo vascular, inicia una cascada de reacciones bioquímicas en el interior de la célula que finaliza en una entrada de calcio en la misma, con la correspondiente contracción de las cadenas de miosina y, por tanto la vasoconstricción.
Se conocen 5 subtipos de receptores muscarínicos denominados M1 a M5, presentes en los diversos tejidos en concentraciones variables y con una afinidad diferente hacia las distintas sustancias. Los M1 a M4 son codificados por los genes m1 a m4, mientras que el quinto ha sido obtenido mediante técnicas de ingeniería genética. Estos receptores muestran una afinidad diferente hacia diversas sustancias: por ejemplo, la pirenzepina es un antagonista muscarínico mucho más potente en los receptores M1 que en los demás receptores y la darifenacina antagoniza de forma más efectiva la acetilcolina en los receptores M3.
Los receptores muscarínicos están íntimamente relacionados con el control de la función de las vías respiratorias. Los receptores M1 facilitan la neurotransmisión colinérgica a través de los ganglios parasimpáticos. Los receptores M2 se localizan en los nervios colinérgicos post-gangliónicos y modulan negativamente la liberación de acetilcolina y su inhibición aumenta la liberación de este neurotransmisor y la broncoconstricción. Los receptores M3 se localizan en el músculo bronquial y en las glándulas mucosas que controlan la respuesta contráctil de las células musculares lisas de las vías respiratorias y la secreción mucosa en respuesta a la acetilcolina. El bloqueo de los estos receptores ocasiona una reducción en la síntesis de la guanosina monofosfato cíclica (cGMP), sustancia que en las vías aéreas reduce la contractilidad de los músculos lisos, probablemente por sus efectos sobre el calcio intracelular.
Las proteínas G acopladas a los receptores muscarínicos tienen, a su vez, una subunidad (subunidad a), crítica para el funcionamiento de los mismos. Existen 4 tipos de proteína G: Gs , Gi , Gq y G12 y las propiedades de los receptores dependen de la naturaleza de la subunidad a la que van acoplados. Las diferentes subunidades de las proteínas G actuand como segundos mensajeros modulando la síntesis de fosfolipadas, AMP-cíclico, fosfatidilinositol, etc.
Aprovechando la diversidad de afinidad de los receptores muscarínicos hacia los diversos ligandos, las diferentes concentraciones de estos receptores en los diversos tejidos, así como otros factores químico-físicos (lipofilia, peso molecular, etc), los farmacólogos y químicos médicos han diseñado y obtenido fármacos cada vez más especificos de los receptores en los órganos diana. Así, desde el uso de los cigarrillos antiasmáticos en el tratamiento del asma o de la tintura de belladona en la incontinencia urinaria se ha recorrido un largo camino hasta los derivados atropínicos broncodilatadores selectivos como el bromuro de tiotropio o los antagonistas de los receptores M3 como la solifenacina o la darifenacina que actuan preferentemente en la vejiga urinaria y se utilizan en la vejiga hiperactiva.
Los anticolinérgicos
inhalados están indicados en el tratamiento de las enfermedades
pulmonares crónicas obstructivas (EPOC) y en el tratamiento del
asma, en este último caso generalmente en combinación
con estimulantes b-adrenérgicos |
|
|
Asma y Enfermedad Pulmonar Obstructiva Crónica
La "Global Initiative on Obstructive Lung Disease" (GOLD) define la EPOC como "una condición patológica caracteriza por una limitación del flujo de aire que no es completamente reversible. Esta limitación del flujo es usualmente progresiva y está asociada a una respuesta inflamatoria anormal a los gases y partículas nocivas". Desde un punto de vista clínico, la EPOC se define sobre una base espirométrica como una reducción del volumen espiratorio forzado en 1 segundo (VEF1) de manera que este es < 80%, con un cociente VEF1/Capacidad vital forzada < 70%, y siendo progresiva en sujetos previamente expuestos a la inhalación de tabaco o de sustancias tóxicas. El asma se define como una condición en la que la limitación del flujo de aire es a menudo reversible, bien espontáneamente, bien mediante un tratamiento farmacológico. La diferencia entre "a menudo reversible" (asma) y "no completamente reversible" (EPOC) puede ser mínima, lo que hace a veces díficil distinguir entre las dos condiciones, en particular en personas mayores o en las que solapan algunas características patológicas.
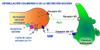
Las patologías del asma y de la EPOC difieren notablemente (*) . En la EPOC la obstrucción de las vías aéreas se encuentra a asociada a una inflamación debida a un aumento de linfocitos T (sobre todo CD8+) macrófagos y neutrófilos. En el asma, la inflamación se encuentra asociada a un aumento de linfocitos T (sobre todo CD4+) y eosinófilos. En consecuencia, la liberación de mediadores y los efectos de estos a nivel de las células bronquiales son diferentes, pero todos ellos originan en último término una inflamación con la correspondiente reducción de la luz de las vías aéreas.
Una importante diferencia entre el asma y la EPOC es la naturaleza de la hipersecreción mucosa asociada a la enfermedad pulmonar obstructiva crónica, un hecho que hasta hace poco tiempo fué considerado como "benigno". Sin embargo, las últimas investigaciones indican que la hipersecreción de moco es un elemento patofisiológico clave tanto en la EPOC como en la bronquiolitis crónica y en el enfisema. Una secreción aumentada de moco puede ocasionar una obstrucción de las vías aéreas (con la correspondientes reducciones de la ventilación/perfusión y del intercambio gaseoso) y/o una reducción del aclaramiento mucociliar (lo que puede inducir una colonización bacteriana y una exacerbación de la bronquitis). Por lo tanto, se consideran importantes los tratamientos terapeúticos o fisioterápicos que permitan el aclaramiento del moco.
Se conoce perfectamente la composición de la mucosidad que recubre las vías respiratorias tanto normales como patológicas. El mucus requiere una óptima combinación en su viscosidad y elasticidad para mantener una eficiente interacción mucociliar. La viscosidad se debe primariamente a las mucinas que son producidas por algunas células del epitelio y por las células mucosas de las glándulas submucosas. Estas mucinas son péptidos altamente glicosilados que pueden unirse entre sí mediante puentes disulfuro para crear un entrecruzamiento de moléculas más o menos complejo y viscoso. Se conocen igualmente los genes que codifican las diversas mucinas (hasta 19 genes en la actualidad) así como se expresan las diversas mucinas tanto en condiciones normales como patológicas (*).
La producción
del mucus está regulada por el sistema nervioso parasimpático
(*).
La estimulación colinérgica de las vías respiratorias
aumenta la secreción de mucinas, electrolitos, agua y albúmina.
La producción de mucina está modulada por el receptor
muscarínico M3 mientras que el M1 regula la secreción
de agua y teóricamente, los anticolinérgicos que bloquean
estos receptores deberían reducir la secreción de mucus.
Al mismo tiempo, al reducir el tono vagal de los músculos lisos
bronquiales deberían facilitar el aclaramiento mucociliar. Sin
embargo, desde el punto de vista clínico estos efectos son díficiles
de evidenciar: el bromuro de oxitropio ha mostrado reducir la secreción
de mucus en pacientes con EPOC, mientras que el bromuro de ipratropio
reduce la tos productiva en comparación con el placebo. Por su
parte, el bromuro de tiotropio no ha mostrado mejorar de forma significativa
el aclaramiento mucociliar en un estudio clínico en el que mejoró
la función ventilatoria. |
|
|
Anticolinérgicos broncodilatadores
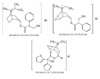
La atropina fué el primer anticolinérgico utilizado en el tratamiento de la enfermedad pulmonar crónica obstructiva, si bien su inespecificidad y su rápida absorción por la mucosa oral y digestiva ocasionaba numerosos efectos secundarios. Por este motivo, se han desarrollado fármacos estructuralmente similares a la atropina, habiéndose introducido en el arsenal terapeútico tres fármacos anticolinérgicos broncodilatadores (*) : el bromuro de ipratropio (1982), el bromuro de oxitropio (1990) y el bromuro de tiotropio (2002). Los tres mantienen unas propiedades farmacológicas similares a las de la atropina, pero con la ventaja de que, al tener una mínima absorción sistémica cuando se administran por vía inhalada, logran un efecto máximo sobre el tracto respiratorio sin apenas efectos secundarios.
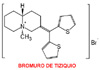
Otros fármacos anticolinérgicos que han sido utilizado esporádicamente en estudios farmacológicos o clínicos en relación con sus efectos sobre los receptores muscarínicos de las vías aéreas son el glicopirrolato (*) (utilizado para reducir la secreción gástrica de ácido), el bromuro de tiziquium (*) (utilizado como astiespasmódico) y el bromuro de fluotropium (*). Ninguno de ellos ha sido introducido posteriormente en la clìnica como broncodilatador.
|
|
Bromuro de Ipratropio
Inicialmente desarrollado para el tratamiento del asma bronquial crónico, el bromuro de ipratropio no es selectivo para los diferentes subtipos de receptores muscarínicos, de manera que ejerce acciones farmacológicas parecidas a las de la atropina sobre los músculos lisos bronquiales, las glándulas salivares, el tracto digestivo y el corazón cuando se administra sistémicamente. Sin embargo, administrado por inhalación, sus efectos se limitan a al tracto respiratorio, siendo dos veces más potente que la atropina como broncodilatador. El bromuro de ipratropio ha sido ampliamente utilizado tanto en el tratamiento del asma como de las enfermedades pulmonares obstructivas. En el primer caso, suele ser menos eficaz que los broncodilatadores b-adrenérgicos, siendo una práctica frecuente asociarlo a uno de ellos (p.ej. el albuterol). El principal inconveniente del bromuro de ipratropio en el asma es su ineficacia en casos de crisis asmáticas y el hecho de que su efecto es relativamente corto (4 a 6 horas) siendo necesarias 2 o 3 administraciones al día.
En 1997 la Sociedad Británica del Tórax (British Thoracic Society) publicó una guía de tratamiento de la EPOC estableciendo que los broncodilatores constituyen la piedra angular del tratamiento asintomático del componente reversible de esta condición. Los agonistas b2-adrenérgicos de corta duración se deben utilizar en primer lugar debido a que proporcionan un rápido alivio de los síntomas. Sin embargo, para una terapia de mantenimiento, se aconseja añadir un broncodilatador colinérgico, debido a que ambos broncodilatadores actúan mediante mecanismos fisiológicos distintos que suelen ser aditivos.
La dosis
recomendada de bromuro de ipratropio es de 20 a 40 mg 3 o 4 veces al
día en la EPOC y de 18 mg 3 o 4 veces al día en la prevención
del broncoespasmo en el asma. |
||
|
El bromuro de oxitropio muestra unas propiedades similares a las del ipratropio, si bien se admite que su efecto es ligeramente más rápido que el del ipratropio. El efecto broncodilatador máximo se alcanza a los 15 minutos de la inhalación. Sin embargo, para mantener los efectos máximos, son necesarias igualmente 3 o 4 administraciones al día. Igual que en el caso del ipratropio, se observan efectos aditivos con los broncodilatadores adrérgicos como por ejemplo el salmeterol (*). Las dosis
recomendadas de bromuro de oxitropio son de 200 mg 3 o 4 veces al día |
|
|
El bromuro de tiotropio es el primer broncodilador colinérgico administrado por inhalación, de larga duración que permite una sola administración al día, lo que representa indudables ventajas en la EPOC. Su larga duración se debe a que el fármaco se une fuertemente a los receptores M3 muscarínicos disociándose lentamente de los mismos. En cambio, el inicio de su efecto es mucho más lento que los del bromuro de ipratropio y de oxitropio, por lo que es inadecuado para el tratamiento de una crisis. Los estudios comparativos con bromuro de ipratropio de un año de duración han demostrado que el bromuro de tiotropio es sustancialmente más eficaz, tanto en lo que se refiere al VEF1 (*), a la disnea (determinada esta última mediante el índice de disnea de Mahler), a la frecuencia del uso de broncodilatadores de rescate (p.ej. salbutamol) y en general en la calidad de vida. La dosis
recomendada es de 18 mg una vez al día administrada mediante
inhalación de polvo seco. |
|
Reacciones adversas y precauciones
Debido a las dosis relativamente pequeñas y a su administración local por inhalación, los tres broncodilatadores anticolinérgicos son muy bien tolerados, siendo raros los efectos secundarios.El más frecuente es la sequedad de boca que suele presentarse entre el 2% (Oxitropio) y 12% (tiotropio) de los pacientes, pero que suele ser moderada y desaparecer espontáneamente sin necesidad de discontinuar la medicación. En el caso del bromuro de ipratropio se observa tos en el 5-5,9% de los casos
Las reacciones alérgicas son raras, manifestándose por urticaria, rash, prurito o edema y se deben a una hipersensibilidad a la atropina y derivados.
Otros efectos anticolinérgicos observados ocasionalmente son retención urinaria, disuria, desórdenes prostáticos, mareos, somnolencia y constipación.
Los tres fármacos pueden aumentar la presión intraocular exacerbando una hipertensión ocular o el glaucoma de ángulo cerrado, siendo necesaria una estrecha vigilancia de estos pacientes. También pueden exacerbar los síntomas de una hiperplasia prostática.
Como ocurre
con todos los fármacos que se administran por inhalación,
los broncodilatores anticolinérgicos pueden inducir un broncoespasmo
paradójico |
||
REFERENCIAS
|
||
| Monografía revisada el 13 defebrero de 2012. Alvaro Galiano. Editor de Medciclopedia | ||
| |
||
  |