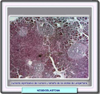
NESIDIOBLASTOSIS [ICD-10: D13.7] |
|
|
||
|
La nesidioblastosis fue descrita por primera vez por George F Laidlaw en 1981, al referirse a la causa más común de hipoglicemia persistente en neonatos. Se caracteriza por una proliferación anormal de las células de los islotes pancreáticos que afecta en forma difusa a la glándula, formando brotes desde el epitelio ductal. Su nombre proviene del griego «nesidia» (islote) y «blasto» (germen). En adultos, su aparición es extremadamente rara. La enfermedad se caracteriza por la aparición de hipoglicemia intensa asociada al ayuno debida a una producción desmedida de insulina, sin tumor pancreático ni intestinal demostrable. Puede presentarse también como un síndrome diarreico crónico asociado a una disminución del peso por hiperproducción de secretina y polipéptido pancreático. Se puede asociar también a pancreatitis crónica, obstrucción ductal pancreática, fibrosis quística, gastrinoma, neoplasia endocrina múltiple (NEM) y a la terapia con sulfonilureas. Etiopatogenia Los recientes avances en los estudios sobre la base molecular de esta enfermedad han puesto de manifiesto la presencia de mutaciones en el canal de potasio ATP-dependiente de los receptores de las sulfonilureas y en la subnidad Kir6.2 del canal rectificador de la corriente de entrada. Estas proteínas son el producto de la expresión de los genes SUR1 y KCNJ11 que se localizan en 11p15.1, 11p15.1. También se han implicado el gen de glucokinasa (GK) y el de la glutamato deshidrogenasa (GLUD1) así como otros todavía sin identificar. Estas mutaciones ocasionan alteraciones histológicas y funcionales de los islotes de Langerhans. Cuando hay mutaciones de los genes GK o GLUD1, la enfermedad tiene un carácter austosómico dominante. En la
nesidioblastosis, las anormalidades histológicas de las estructura
pancreáticas se agrupan en hiperplasia adenomatosa focal y anormalidades
difusas de los islotes. (*)
Como consecuencia de estas anomalías, se produce un fallo en
la secreción de insulina, no siendo capaces los islotes de reconocer
la presencia de hipoglucemia y, por lo tanto, de reducir la secreción
de insulina. Los niveles de insulina circulante demasiado elevados promueven
la glucogénesos hepática y muscular, causando una reducción
de los niveles de glucosa en sangre y la supresión de la formación
de ácidos grasos como alternativa energética. El resultado
final es una severa hipoglucemia con graves alteraciones neurológicas,
que pueden llegar a convulsiones cuando los niveles de glucosa caen
por debajo de de 20-30 mg/dL
|
|
Diagnóstico(*) La mayor parte de los pacientes presenta al poco de nacer síntomas de hipoglucemia (hambre desmedida, nerviosismo, letargia, apnea y diaforesis). Los niños algo mayores presentan además diaforesis y cambios de humor. En los adultos, se observan cefaleas, mareos, síncopes y pérdida del conocimiento que se agravan en ayunas y mejoran al comer. La hipoglucemia es persistente y requiere la administración continua de alimentos o de glucosa. El diagnóstico de la nesidioblastosis es a menudo difícil debido al pequeño tamañ de las lesiones. La arteriografia puede contribuir al diagnóstico y la ecografía durante la cirugía es importante para identificar lesiones múltiples Se debe plantear la presencia de una nesidioblastosis toda vez que no se encuentre tumor en la imagenología convencional ni en la exploración quirúrgica, teniendo en cuenta que la biopsia por congelación tiene un valor dudoso en su diagnóstico intraoperatorio. Usualmente, los pacientes no presentan en la exploración ninguna señal o síntoma característicos cuando están en condiciones euglucémicas. La presencia de hepatomegalia sugiere una desorden metabólico como galactosemia, enfermedades de almacenamiento del glucógeno o fructosemia.
|
||
 |
TRATAMIENTO (*) El tratamiento inicial consistirá en el control de la hipoglucemia mediante la infusión de glucosa. Los corticoides inducen la glucogenesis y pueden ser útiles para el control de los niveles de glucosa a corto plazo. La diazoxida es un agente antihipertensivo que relaja los músculos lisos de las arteriolas periféricas y, aunque está químicamente emparentado con las tiazidas, no tiene efectos diuréticos. La diazoxida inhibe la secreción pancreática de insulina y favorece la secreción hepática de la glucosa. Sin embargo, este fármaco produce retenciones de agua y sodio y debe ser utilizado con precaución en pacientes con insuficiencia cardiaca. La octeotride, un análogo de la somatostatina inhibe la secreción de insulina, y resulta eficaz a corto plazo. Sin embargo, con el tiempo, los pacientes desarrollan tolerancia y la octeotride ha sido asociada a un retraso del crecimiento y otras reacciones adversas. La resección
corporocaudal del páncreas en la gran mayoría de los casos
bastará para controlar sus manifestaciones clínicas, a
pesar de que en un porcentaje mínimo de pacientes resecados persiste
la hipoglicemia de ayuno, que responde bastante bien a la diazoxida. |
|
REFERENCIAS
|
||
Monografía creada: 16 de Septiembre, 2004. Equipo de Redacción de IQB |
||
| |